Olá meus queridos alunos! Hoje estudaremos a água. Boa aula.
Galera! A água é a substância mais abundante dentro e fora do corpo dos seres vivos. O surgimento e a manutenção da vida tem muito haver com a água. Agora vamos analisar algumas características e importância da água. Galera! Nessa aula não falarei dos estados físicos da água. Porque ela já foi explicada numa aula sobre os estados físicos da matéria nesse blog. Acesse e confira.
A aguá tem uma mega importância na manutenção da vida no planeta Terra. Muita atividades de seres vivos depende da água. O nosso próprio corpo é formado entre 60 a 75% de água corporal. Um embrião humano tem cerca de 90% de água corporal. Agora observe a quantidade de água no planeta Terra:
Observe o quadro e analise a importância da água. E sua quantidade disponível em alguns órgãos do nosso corpo.
Galerinha! Observaram. Não deixem de beber água. Esses são alguns benefícios da água entre outras mais. Agora vamos estudar a fórmula molecular da água e suas características.
Fórmula molecular da água.
A fórmula molecular da água é constituída por dois átomos de hidrogênio (H) e um átomo de oxigênio (O), conforme o esquema abaixo.

Modelo molecular da água.
Galera! O modelo molecular da água é representado por esse desenho abaixo. Galerinha, observe que os átomos de hidrogênio em azul é de carga positiva. E o oxigênio em vermelho é negativo. Então dizemos que a água é uma substância polar por que tem zona positiva e zona negativa.
Observe o quadro:
Muito fácil né galerinha. Agora vamos analisar outras características.
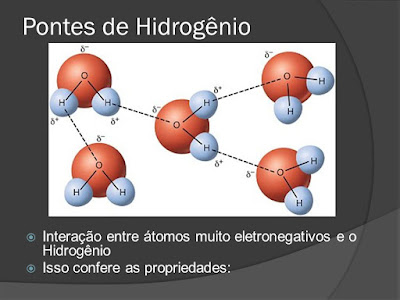
Ligação de Hidrogênio.
Observação: A palavra pontes de hidrogênio está em desuso. O correto é ligação de hidrogênio.
Observação: A palavra pontes de hidrogênio está em desuso. O correto é ligação de hidrogênio.
A água realiza ligações químicas com outras moléculas de água, por causa da atração entre cargas elétricas opostas.
Observe o esquema:
Galera! O oxigênio negativo liga-se com o hidrogênio positivo formando a ponte de hidrogênio.
O hidrogênio positivo liga- se ao oxigênio negativo formando a ponte de hidrogênio e assim por diante conforme o desenho abaixo.
Galera! Outro esquema abaixo mostrando a ligação entre o oxigênio (-)e o hidrogênio (+) que são cargas opostas. A forte atração entre as moléculas d' água é chamada de coesão.
Coesão é a forte atração entre as moléculas d' água.
Tensão superficial.
A coesão entre as moléculas d' água é responsável pela tensão superficial da água. E por causa dessa propriedade os insetos conseguem andar e pousar sobre a água. observe o desenho abaixo.
Imagem real de um inseto pousado n' água.
Imagem real de uma libélula pousada n' água.
Imagem real de uma aranha pousada n' água.
Observe a explicação do quadro abaixo.
Galera! Observaram. Além de conseguirem pousar n' água, os animais conseguem até correr sobre a água. Observe esses lagarto correndo sobre a água. Incrível.
Que imagens mais lindas.
Uma outra propriedade da água é o poder que ela tem de associar- se a outras substâncias polares e conseguir dissolve- la. Observe o quadro.
Galerinha! Á água é considerada um solvente universal. No esquema abaixo temo um copo com água que é um solvente. E nesse copo é colocado um soluto, por exemplo um açúcar.
O solvente água dissolve o soluto açúcar, formando uma solução.
Água e óleo.
Galerinha! Á água não se mistura com os óleos. Devido as suas polaridades. Neste caso:
Á água é uma substância POLAR que não se liga e se mistura ao óleo, que é uma substância APOLAR.
Galerinha! Espero que tenham entendido. Obrigado por estudar mais uma aula.
Profº Weslei.